
Главная
страница
Сведения об
авторах
Выход перекиси водорода и ионов меди при обработке воды диафрагменным электрическим разрядом
Суворов И. Ф., Юдин А. С., Улейчик К. А., Читинский государственный университет, Чита, Россия
Большим количеством исследований показано наличие бактерицидных свойств и эффекта последействия растворов, обработанных диафрагменным электрическим разрядом (ДЭР) с применением медных электродов. Приобретенные особенности сохраняются в течение длительного времени (одна неделя и более). По мнению одних исследователей, основной фактор возникновения эффекта последействия — наличие в обработанной воде продуктов эрозии медных электродов. По мнению других, возможно влияние таких компонентов, как радикалы ОН•, перекись водорода, ионы меди. Во многих работах показано, что один из основных обеззараживающих компонентов — перекись водорода, образующаяся в достаточных количествах в зоне разряда. Ее появление обусловлено в первую очередь реакциями между озоном и радикалами OH•, а также димеризацией радикалов.
В настоящем исследовании дана оценка выхода ионов меди и перекиси водорода в обработанной ДЭР воде в зависимости от ее химического состава. Пробные эксперименты по получению H2O2 проводили на модельном растворе K2SO4 в статическом режиме (без движения жидкости через диафрагму).
Продолжительность разряда 2 мин. Более длительное воздействие приводило к сильному нагреву жидкости и ее вскипанию.
Характеристики диафрагмы: толщина 5 мм; количество отверстий 5; диаметр отверстий 3 мм. В экспериментах использовали угольные и медные электроды, напряжение на которых изменяли от 200 до 1 200 В.
При более низком напряжении разряд отсутствовал, а при более высоком обрабатываемая жидкость сильно нагревалась и вскипала, а разряд из квазиимпульсного режима переходил в дуговой, что вызывало разрушение диафрагмы.
Электропроводность дистиллированной воды доводили до 0,45 мСм/см. Контролировали ее с использованием измерителя параметров воды Hanna HI9813-6. Перекись водорода определяли титрованием с перманганатом калия. Результаты экспериментов приведены на рис. 1.
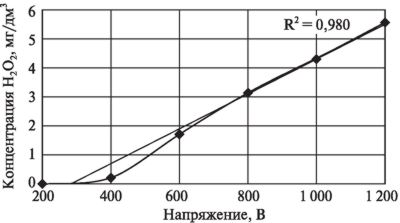
Рис. 1. Зависимость концентрации перекиси водорода в модельном растворе K2SO4, обработанном ДЭР, от приложенного напряжения
Перегиб графика при 400 В и последующий быстрый рост концентрации перекиси водорода с повышением приложенного напряжения объясняется появлением устойчивого разряда по всем отверстиям и переходом его от апериодического режима к квазиимпульсному. Для последнего характерна почти линейная зависимость концентрации перекиси водорода от приложенного напряжения (в диапазоне от 400 до 1 200 В).
Для изучения влияния химических элементов, присутствующих в питьевой воде, на выход ионов меди и перекиси водорода, проведен ряд экспериментов по обработке ДЭР модельных растворов с электропроводностью 0,45 мСм/см при напряжении на электродах 1 200 В. Результаты представлены на рис. 2.
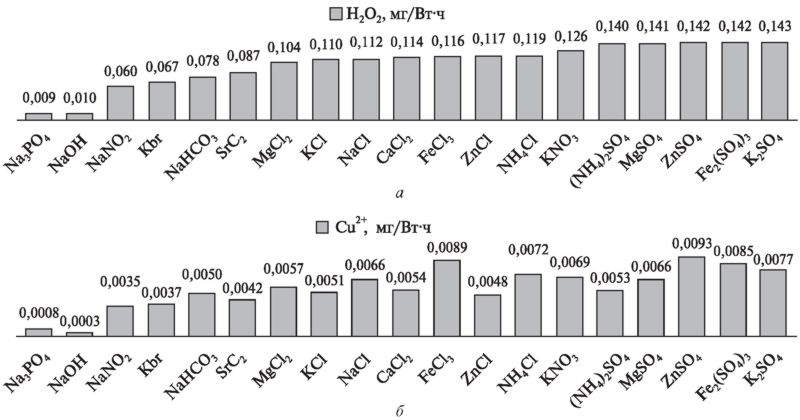
Рис. 2. Диаграммы выхода перекиси водорода (а) и ионов меди (б) в зависимости от химического состава модельных растворов
Анализ диаграмм показывает, что выход перекиси водорода и ионов меди в большей степени зависит от pH среды, чем от химического состава растворов: Na3PO4 и NaOH создают наиболее щелочную среду, в которой наблюдается наименьший выход продуктов разряда. Незначительное понижение выхода продуктов разряда, не зависящее от значений pH, наблюдается также в присутствии анионов Cl-. Аналогичную картину можно ожидать при наличии других галогенид-анионов — фтора, брома, йода.
Анализ полученных данных позволяет сделать следующий вывод. В наибольшей степени выход ионов меди и перекиси водорода уменьшают соединения, создающие в растворе щелочную среду, а в наименьшей — создающие кислую среду. Для проверки полученного результата проведен эксперимент по обработке модельных растворов с различным значением pH. В дистиллированную воду в различных пропорциях добавляли ацетатный буфер. Сульфатом калия электропроводность полученных модельных растворов доводили до необходимого уровня.
Результаты эксперимента представлены на рис. 3.
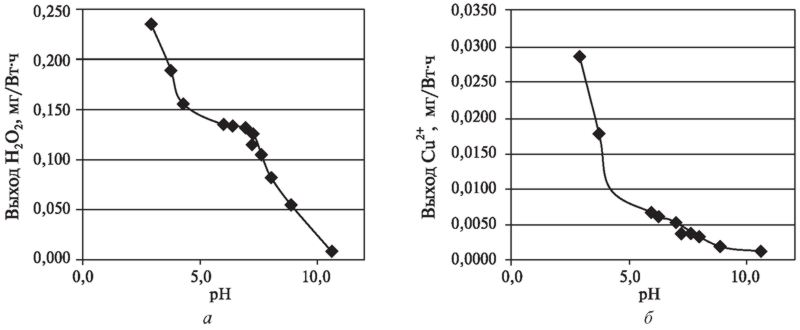
Рис. 3. Зависимость выхода перекиси водорода (а) и ионов меди (б) от реакции среды
Полученные данные подтвердили вывод о характере влияния реакции среды на выход перекиси водорода и ионов меди. В диапазоне pH от 4,5 до 8,0 на обоих графиках наблюдается пологий участок, более выраженный для перекиси водорода.
Таким образом, для получения дезинфицирующего агента следует использовать воду с низким значением pH. При рН выше 8,0 процесс становится неэффективным.
Присутствие карбонат-ионов приводит к достаточно большому (~50 %) снижению выхода как ионов меди, так и перекиси водорода по сравнению с наибольшим значением в данной серии опытов для K2SO4 (см. рис. 2). Это может быть связано не только с повышением щелочности раствора, но и со склонностью ионов CO32− к пассивации поверхности электродов, что вызывает снижение выхода ионов меди. Кроме того, карбонат-ионы могут связывать гидроксил-радикалы:
CO32− + •OH → •CO3− + OH−.
В результате уменьшается концентрация перекиси водорода. Хотя радикал •CO3− также является окислителем, его активность намного ниже, чем гидроксил-радикала. Подобную картину можно ожидать и в присутствии ионов PO42−.
Результаты настоящего исследования использованы при усовершенствовании системы обеззараживания сточных вод в п.г.т. Новоорловск Забайкальского края.
Hydrogen Peroxide and Copper Ion Generation by Diaphragm Electric
Discharge in WaterSuvorov I. F., Yudin A. S., Uleychik K. A., Chita State University, Chita, Russia
This paper provides an estimate of copper ion and hydrogen peroxide output in water treated by diaphragm discharge water. The main finding is that the generation of copper ions and hydrogen peroxide is more significantly affected by pH and less significantly — by the chemical composition of water. The results of this research have been used to enhance the existing disinfection system in the Novoorlovsk Town (Zabaykalskiy Krai).
Суворов Иван Флегонтович,
д-р техн. наук, проф., кафедра
электроснабжения, Читинский государственный университет, ул. Баргузинская, 49,
Чита, 672039, Россия. Тел./факс (3022) 41-69-66, моб. (924) 277-66-40.
E-mail
Юдин Артем Сергеевич,
канд. техн. наук, доц., кафедра
электроснабжения, Читинский государственный университет, ул. Баргузинская,
49, Чита,
672039,
Россия. Тел./факс (3022) 41-69-66.
E-mail
Улейчик Ксения Анатольевна,
канд. техн. наук, доц., кафедра
электроснабжения, Читинский государственный университет, ул. Баргузинская, 49,
Чита, 672039, Россия. Тел./факс (3022) 41-69-66.
E-mail
© Независимое
агентство экологической
информации
Последние изменения внесены
02.04.11