Главная
страница
Сведения об авторах
ПЕРЕРАБОТКА СЕРЕБРОСОДЕРЖАЩЕГО ВТОРИЧНОГО СЫРЬЯ
Байрачный Б. И., Ляшок Л. В., Орехова Т. В., Горовая Т. Н., Национальный технический университет «Харьковский политехнический институт», Харьков, Украина
Важным аспектом проблемы комплексной переработки отходов является охрана окружающей среды. Металлосодержащее вторичное сырье, с одной стороны, наносит огромный вред окружающей среде, с другой — представляет собой ценнейший ресурс, по содержанию полезных компонентов в сотни и тысячи раз превосходящий природные источники.
Приоритетным направлением является переработка сырья, содержащего драгоценные металлы. По прогнозам за счет переработки промышленных отходов годовая потребность Украины в серебре может быть обеспечена на 10–25 %.
На кафедре технической электрохимии НТУ «ХПИ» разработаны технологии извлечения благородных металлов из различных видов вторичного сырья, в том числе электронного лома. Анализ состава дает основание отнести его к классу неоднородного полиметаллического сырья, содержащего различные химические элементы (таблица). Благородные металлы могут содержаться в таком материале в виде плакировки, припоя, гальванических покрытий, а основа может быть металлической и неметаллической.
Состав электронного лома
|
Вид электронного лома |
Содержание, мас. % |
|||||
|
Au |
Ag |
МПГ |
Пластик |
Керамика |
Стекло |
|
|
Микросхемы
|
0,01–0,1 |
0,03–0,3 |
0,005–0,03 |
40–60 |
До 5 |
– |
|
Микросхемы
|
1–7 |
0,04–5 |
0,02–0,15 |
– |
90–99 |
– |
|
Радиолампы |
0,001–0,07 |
0,01–1,5 |
8∙10–5–4∙10–3 |
До 5 |
– |
20–30 |
|
Радиодетали |
0–0,4 |
0,001–6 |
– |
– |
– |
– |
|
Разъемы |
0,3–1 |
0,5–5 |
– |
80–90 |
– |
– |
|
Контакты |
0,001–0,16 |
0,04–5 |
– |
До 10 |
– |
– |
Общая схема переработки вторичного сырья, содержащего драгоценные металлы,
предполагает такую последовательность операций:
– гомогенизация сырья и отбор предварительной пробы;
– анализ пробы для расчета с поставщиками и выбор метода переработки в
зависимости от состава материала;
– подготовка сырья, связанная с его предварительным обогащением, отделением
неметаллических составляющих, выделением магнитной и немагнитной фракции и т.
д.;
– извлечение благородных металлов, как правило в концентраты, пиро- и
гидрометаллургическими методами или сочетанием этих процессов.
Согласно анализу работ в области пиро- и гидрометаллургии вторичного сырья, содержащего благородные металлы, гидрометаллургические процессы предпочтительнее. Они предполагают операции химического вскрытия сырья, предварительного концентрирования и разделения и получение кондиционных по чистоте продуктов.
Авторами разработана технология извлечения серебра из отходов, в частности электронного лома, с получением в качестве конечного продукта серебряного порошка однородного гранулометрического состава чистотой 99,99 %, что соответствует ДСТУ 6836–04.
Предварительной операцией является механическая подготовка серебросодержащих отходов к металлургическому переделу и обезжиривание поверхности сырья в растворе, содержащем ПАВ и кальцинированную соду.
Гидрометаллургический процесс предполагает растворение сырья в водном растворе с применением минеральных и органических реагентов. В зависимости от состава материала и применяемых реагентов возможно селективное отделение примесей от благородных составляющих либо полный перевод всех компонентов в раствор.
Возможность осуществления селективного растворения (выщелачивания) благородных металлов определяется величиной изменения энергии Гиббса ∆G и константы равновесия Кр реакции выщелачивания. При больших отрицательных значениях ∆G константа равновесия реакции очень велика, и реакция практически необратима. Положительные значения ∆G свидетельствуют о том, что реакция практически не идет, так как величина Кр очень мала. Например, при растворении серебряного покрытия с поверхности латунного электронного лома в растворе H2SO4 с концентрацией 14,56 моль/дм3 при 80 °С ∆G = –119,9 кДж/моль, а Кр = 1,36 ∙ 10–11. Следовательно, реакция необратимо протекает в сторону растворения серебряного покрытия. Исходя из рассчитанных величин ∆G и Кр выбирается оптимальный температурный режим проведения процесса.
На практике, кроме возможности протекания процесса, необходимо установить
зависимость его скорости (кинетики) от различных технологических параметров. При
изучении кинетики процессов выщелачивания экспериментально определяют
зависимость степени выщелачивания от продолжительности процесса при различных
температурах и концентрациях реагентов. Степень выщелачивания описывается
уравнением α = (G0 — G)/G0, где G0
и G — начальное и текущее содержание
выщелачиваемого металла в сырье.
На рисунке показана зависимость степени выщелачивания серебра в растворе H2SO4 с концентрацией 14,56 моль/дм3 от длительности процесса при различных температурах.
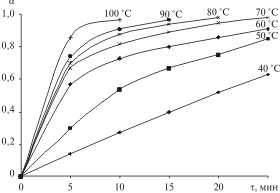
Зависимость степени выщелачивания серебра в растворе с концентрацией H2SO4 14,56 моль/дм3 от длительности процесса при различных температурах
На основании экспериментально полученных зависимостей α = f(τ) рассчитывается энергия активации процесса, порядок реакции по реагенту и определяется лимитирующая стадия процесса. Так, при растворении серебра с поверхности латунного лома в растворе H2SO4 при 80 °С энергия активации процесса и порядок реакции по серной кислоте равны соответственно Е = 15,3 кДж и n = 1. Это свидетельствует о том, что процесс протекает в диффузионной области и для его интенсификации следует использовать механическое перемешивание или метод перколяции — циркуляцию раствора сквозь неподвижный слой сырья.
В ряде случаев после извлечения компонентов исходного сырья в раствор в качестве последующей операции используют осаждение труднорастворимых соединений, что позволяет провести избирательное осаждение основного металла или очистить раствор от примесей. Для селективного извлечения серебра из раствора проводят осаждение труднорастворимого AgCl раствором NaCl.
Одной из актуальных задач современной науки и техники является получение различными методами металлов высокой степени чистоты.
Для получения высокочистых металлов широко применяются электрохимические методы. При электрохимическом извлечении серебра из растворов выщелачивания на катоде получают серебряный порошок чистотой 99,99 %. Последующее электрохимическое рафинирование позволяет провести дополнительную очистку.
Для получения серебряных порошков возможно использование различных режимов электролиза. Наиболее широко в промышленности используется гальваностатический режим, но порошок, полученный в таких условиях, имеет широкий спектр распределения частиц по размеру.
Авторами изучена возможность получения порошка серебра при потенциостатическом режиме электролиза и сделан вывод, что такой режим обеспечивает наибольшую стабильность осаждения металлического порошка, а следовательно, и однородность его гранулометрического состава. При потенциостатическом электролизе из электролита, содержащего NH3 0,24 моль/дм3 (25 %), (NH4)2SO4 0,38 моль/дм3 и серебра 0,019–0,092 моль/дм3, получен мелкодисперсный серебряный порошок, в котором более 60 % частиц имеют размеры до 250 мкм.
Полученный порошок серебра может использоваться в медицине, порошковой
металлургии, электротехнической промышленности для изготовления контактов
электропусковой аппаратуры, серебряных припоев.
RECOVERY OF ARGENTIFEROUS RECYCLABLE MATERIAL
Bayrachniy B. I., Lyashok L. V., Orekhova T. V., Gorovaya T. N., National
Technical University
«Kharkiv Polytechnic Institute», Kharkiv, Ukraine
The method of extraction of silver from the electrotechnical scrap is proposed.
Composition of the electrotechnical scrap is analyzed, basic operations of
technological process are considered.
Байрачный Борис Иванович, д-р техн. наук,
проф., зав. кафедрой технической электрохимии, Национальный технический
университет «Харьковский политехнический институт», ул. Фрунзе, 21, Харьков,
61002, Украина. Тел. (057) 707-63-95
Ляшок Лариса Васильевна, канд. техн. наук, доц., кафедра технической
электрохимии, Национальный технический университет «Харьковский политехнический
институт», ул. Фрунзе, 21, Харьков, 61002, Украина. Тел. (057) 707–67–91
Орехова Татьяна Васильевна, вед. инженер, кафедра технической
электрохимии, Национальный технический университет «Харьковский политехнический
институт», ул. Фрунзе, 21, Харьков, 61002, Украина. Тел. (057) 707–67–91
Горовая Татьяна Николаевна, аспирант, кафедра технической электрохимии,
Национальный технический университет «Харьковский политехнический институт», ул.
Фрунзе, 21, Харьков, 61002, Украина. Тел. (057) 707-67-91
© Независимое агентство экологической информации
Последние изменения внесены 22.09.08